
Prueba de CAMP positiva para Listeria monocytogenes. Fuente: Benadof, Dona. (2008). Listeria monocytogenes. Revista chilena de infectología, 25(5), 350. https://dx.doi.org/10.4067/S0716-10182008000500005
FUNDAMENTOS
Para esta prueba se utilizan cepas de Staphylococcus aureus y Rhodococcus equi productoras de betalisina. Algunas especies de Listeria producen una proteína extracelular (factor CAMP), la cual actúa sobre los eritrocitos en forma sinérgica con la betalisina. Se pueden emplear placas de agar sangre ovina, pero es preferible usar el método de la doble capa.
MEDIO PARA CAPA BASAL *
Ingredientes
Agar base sangre Nº 2 ...........................................240 g
Agua destilada...................................................... 1000 ml
Preparación del medio
Disolver la base deshidratada en agua destilada mediante ebullición. Ajustar pH a 7. Transferir a tubos o frascos. Esterilizar durante 15 minutos a 121 ºC. Enfriar a 45 ºC
MEDIO SANGRE OVINA **
Ingredientes
Medio basal ..............................................................100 ml
Sangre ovina desfibrinada estéril .......................7 ml
Preparación del medio
Agregar sangre ovina al medio base estéril y fundido.
MEDIO COMPLETO
Preparación del medio
Distribuir 10 ml de medio basal* en placa para forma una capa. Dejar solidificar. Agregar 3 ml del medio sangre ovina**, para formar capa muy fina.
Advertencia: Si el medio con sangre se agrega a placas de medio basal preparadas anteriormente, es necesario colocarlas previamente en estufa a 36 ºC durante 20 minutos antes de agregar la capa fina con sangre.
Cultivos patrones
Staphylococcus aureus NCTC 1803 Rhodococcus equi NCTC 1621
Mantenimiento: Cultivar en estrías, incubar a 36 ºC. Subcultivar cada treinta días.
REALIZACIÓN DE LA PRUEBA
Trazar una línea de Staphylococcus aureus a lo largo de la placa y otra paralela y alejada de Rhodococcus equi, en forma de inóculo fino. De igual manera sembrar perpendicularmente a las cepas patrones los cultivos incógnita que se desean probar, sin tocar la línea del S. aureus ni al R. equi, pero a distancia aproximada de 5 mm.
Pueden probarse simultáneamente varias cepas en la misma placa. Si se emplea el método de doble capa, incubar a 36 ºC durante 12-18 horas. Si se hiciera la prueba en monocapa de agar sangre, incubar a igual temperatura durante 24 horas.
LECTURA E INTERPRETACIÓN
Reacción positiva con S. aureus: zona de beta-hemólisis estimulada en la intersección de la cepa incógnita. Se observa como una pequeña zona redondeada de hemólisis. Si se observa una zona pequeña con R. equi, se considera negativa.
Reacción positiva con R. equi: zona ancha en forma de cabeza de flecha.
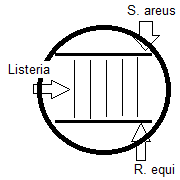
Modelo de inoculación en placa de agar sangre de carnero:
Las líneas horizontales representan las estrías de S. aureus (S) y R. equi (R).
Las líneas verticales representan las estrías de los aislamientos que posiblemente son Listeria.
Las líneas intersectadas indican las regiones de aumento de la hemólisis.
CONTROL DE LA CALIDAD
Control positivo: Listeria monocytogenes ATCC 19111; ATCC 13932
Control negativo: Listeria innocua ATCC 33090
Fuente: Servicio Bacteriología Especial Departamento de Bacteriología Instituto Nacional de Enfermedades Infecciosas A.N.L.I.S. “Dr. Carlos G. Malbrán” (2008). Manual de Procedimientos Aislamiento, identificación y caracterización de Listeria monocytogenes. Buenos Aires: Callejo, R. , Prieto, M. , Martínez, C. , Aguerre, L. , Rocca, F. y Martínez G.
listeria, pruebas bacteriológicas, bacilos g+, prueba de camp
- Visto: 12972


